Калиум тиоцијанат
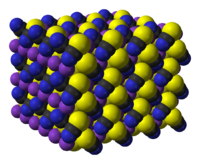
Калиум тиоцијанат ― хемиско соединение со молекуларна формула KSCN. Тоа е важна сол на тиоцијанатски анјон, еден од псевдохалидите. Соединението има ниска точка на топење во однос на повеќето други неоргански соли.
| |

| |
Други називи Калиум сулфоцијанат | |
| Назнаки | |
|---|---|
| 333-20-0 | |
| Бајлштајн | 3594799 |
| ChEBI | CHEBI:30951 |
| ChemSpider | 9150 |
| EC-број | 206-370-1 |
| 21362 | |
| |
| 3Д-модел (Jmol) | Слика |
| PubChem | 516872 |
| RTECS-бр. | XL1925000 |
| |
| UNII | TM7213864A |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | Безбојни накај течни кристали |
| Мирис | Без мирис |
| Густина | 1.886 g/cm3 |
| Точка на топење | |
| Точка на вриење | |
| 177 g/100 mL (0 °C) 217 g/100 mL (20 °C) | |
| Растворливост | ацетон: 21.0 g/100 mL етанол: растворлив |
| −48.0·10−6 cm3/mol | |
| Опасност | |
| GHS-ознаки: | |
Пиктограми
|
 
|
Сигнални зборови
|
Внимание |
Изјави за опасност
|
H302, H312, H318, H319, H332, H412 |
Изјави за претпазливост
|
P261, P264, P270, P271, P273, P280, P301+P312, P302+P352, P304+P312, P304+P340, P305+P351+P338, P310, P312, P322, P330, P337+P313, P363, P501 |
| NFPA 704 | |
| Смртоносна доза или концентрација: | |
LD50 (средна доза)
|
854 mg/kg (преку уста)[1] |
| Безбедносен лист | ICSC 1088 |
| Слични супстанци | |
| Други анјони | Калиум цијанат Калиум цијанид |
| Други катјони | Натриум тиоцијанат Амониум тиоцијанат |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Употреба во хемиска синтеза
уредиВодениот KSCN реагира речиси количински со Pb(NO3)2 за да добие Pb(SCN)2, кој е користен за претворање на ацил хлориди во изотиоцијанати.[2]
KSCN го претвора етилен карбонатот во етиленсулфид.[3] За таа цел, KSCN прво е топен под вакуум за да се отстрани водата. Во поврзаната реакција, KSCN го претвора циклохексен оксидот во соодветниот еписулфид.[4]
- C6 H10O + KSCN → C6H10S + KOCN
KSCN е исто така почетниот производ за синтеза на карбонил сулфид.
Други употреби
уредиРазредениот воден KSCN повремено е користен за умерено реалистични ефекти на крвта однсно сценската крв во филмот и театарот. Може да е нанесено на површина или да се чува како безбоен раствор. Кога е во допир со раствор на железен хлорид (или други раствори што содржат Fe3+), производот од реакцијата е раствор со крваво црвена боја, поради образувањето на комплексот тиоцијанатоирон јон. Така оваа хемикалија често е користена за да се создаде ефект на „стигма“. Бидејќи и двата раствора се безбојни, може да се постават посебно на секоја рака. Кога рацете ќе дојдат во допир, растворите реагираат и ефектот изгледа неверојатно како стигмата.[се бара извор]
Слично, оваа реакција е користена како тест за Fe3+ во лабораторија.
Наводи
уреди- ↑ Chambers, Michael. „ChemIDplus - 333-20-0 - ZNNZYHKDIALBAK-UHFFFAOYSA-M - Potassium thiocyanate [NF] - Similar structures search, synonyms, formulas, resource links, and other chemical information“. chem.sis.nlm.nih.gov. Посетено на 22 февруари 2023.
- ↑ Smith, P. A. S.; Kan, R. O. (1973). „2a-Thiohomophthalimide“. Organic Syntheses.; Collective Volume, 5, стр. 1051
- ↑ Searles, S.; Lutz, E. F.; Hays, H. R.; Mortensen, H. E. (1973). „Ethylenesulfide“. Organic Syntheses.; Collective Volume, 5, стр. 562
- ↑ van Tamelen, E. E. (1963). „Cyclohexenesulfide“. Organic Syntheses.; Collective Volume, 4, стр. 232
