Хемоглобин
Хемоглобинот е респираторниот пигмент на ‘рбетниците. Од него потекнува црвената боја на еритроцитите, а со тоа и на крвта. Тој претставува сложена белковина кој се состои од белковинска компонента глобин и простетична група хем. Скратено се обележува со Hb. Молекулската маса на хемоглобинот изнесува 67.000. Белковинската компонента е составена од четири полипептидни ланци, и тоа два α и два β. Секој од нив содржи по една простетична група (хем), така што во молекулата на хемоглобинот има исто така и четири хема.
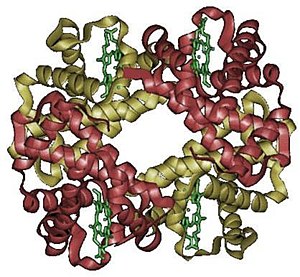

Железото во хемоглобинот се наоѓа во облик на двовалентен јон Fe++. Со една координативна врска, железото во секој хем е поврзано со глобинот преку аминокиселината хистидин. Покрај тоа, и две карбоксилни групи од пропионската киселина на хемот се сврзани за глобинот.
Видови хемоглобин
уредиХемоглобините на различните животни имаат иста простетична група (хем), но белковинската компонента (глобин) е со различен состав, специфичен за поодделните видови. Според тоа, и исти видови на животни содржат различни хемоглобини. Така на пример, во крвта на возрасен човек се наоѓаат два вида на хемоглобин: адултен хемоглобин (HbA) и хемоглобин A2 (HbA2). И двата се состојат од четири полипептидни ланци, и тоа хемоглобинот А од два α и два β, а хемоглобинот А2 од два α и два δ. Хемоглобинот на човековиот фетус содржи фетален хемоглобин (HbF), кој е составен од два α и два γ полипептидни ланци. α ланецот се состои од 141 аминокиселина, а β, γ и δ од 146. Последните три се разликуваат по тоа што на одделни места на полипептидниот ланец имаат различни аминокиселини.
Физички својства
уредиХемоглобините и нивните деривати имаат карактеристични апсорпциони спектри, така што можат лесно да се идентификуваат. Хемоглобините на различни животни кристализираат во различни кристални облици и различно се раствораат.
Функција
уредиКај животинските организми хемоглобинот има респираторна функција. Оваа физиолошки најважна особина на хемоглобинот се основа на тоа што тој се соединува со воздушниот кислород при што се добива лабилно соединение оксихемоглобин. Во оксихемоглобинот, молекулата на кислородот е координативно сврзана за железото од хемот кое не ја менува својата валентност, туку останува двовалентно. Оксихемоглобинот е молекулско соединение на хемоглобинот со кислородот, а не оксидационен производ на хемоглобинот. Процесот се нарекува оксигенација. Секој атом на железо врзува по една молекула на кислород, а бидејќи во хемоглобинот има четири хема, реакцијата на респирација е следна:
Оксигенацијата на хемоглобинот, миоглобинот и еритрокурионот е повратна реакција која има своја константа на рамнотежа. За полесно разбирање, тука ќе биде претставена оксигенацијата на миоглобинот (Mb), кој има еден атом на железо и сврзува една молекула на кислород кога образува оксимиоглобин. Реакцијата на миоглобинот со кислородот е:
Константата на рамнотежа за реакцијата е:
Концентрацијата на кислородот е пропорционална со неговиот делумен притисок и затоа наместо O2, може да се напише pO2:
- или , а за хемоглобинот
Се добива дека односот на концентрацијата на оксимиоглобинот и миоглобинот зависи од делумниот притисок на кислородот. Тоа важи и за хемоглобинот. Со зголемување на притисокот на кислородот се зголемува и концентрацијата на оксихемоглобинот, а се смалува концентрацијата на хемоглобинот и обратно.
Оксихемоглобинот е слаба киселина која со зголемувањето на концентрацијата на водородни јони во средината дисоцира на хемоглобин и кислород. Со зголемување на концентрацијата на CO2 во ткивата, кое е проследено и со зголемување на концентрацијата на водородни јони, поволно влијае, покрај намалениот pO2, на ослободување на кислородот од оксихемоглобинот.
Хемоглобините на различни животни имаат различен афинитет кон кислородот. Така, хемоглобинот на луѓето има поголем афинитет од кучешкиот или кокошкиниот.
Хемоглобинот како пуфер
уредиХемоглобинот, како и сите белковини, има својства на пуфер. Бидејќи во крвта има најмногу хемоглобин (10-14 g%), до 60% од пуферскиот капацитет на крвта доаѓа од хемоглобинот. Во ткивата се ослободуваат толку молекули на CO2 колку што pH на крвта би требало да се смали од 7,4 на 4,0, а тоа не се случува. Хемоглобинот и оксихемоглобинот имаат изоелектрична точка при pH од 6,8, односно 6,65. При pH на крвта, тие се однесуваат како слаби киселини кои реагираат со катјоните и притоа даваат соли: карбохемоглобин (KHb) и карбоксихемоглобин (KHbO2). Кога на овие соли се делува со јаглеродна киселина, се ослободува хемоглобинот, а јаглеродната киселина преминува во бикарбонат:
Во крвта, најголем дел од јаглеродниот диоксид се наоѓа во вид на бикарбонат и pH на крвта останува константна.
Покрај тоа што хемоглобинот како пуфер спречува да не дојде до промена на концентрацијата на водородни јони во крвта, тој исто така еден дел од CO2 го сврзува за глобинот, давајќи карбаминохемоглобин:
Во белите дробови, со дејството на посилната киселина оксихемоглобин на карбаминохемоглобинот, се ослободува CO2 од неговата молекула и тој преминува во хемоглобин.
Во историјата, уметноста и музиката
уредиИсториски, бојата на крвта била асоцирана со `рѓа, какошто Старите Римјани ја асоцирале планетата Марс со богот на војната, бидејќи Марс е портокалово-црвен. Бојата на Марс потекнува од железните оксиди на неговата почва, но црвеноста на крвта не потекнува од хемоглобинот и неговите оксиди, што е често, но погрешно верување. Крвта е црвена заради порфиринот, функционална група на хемоглобинот за кој е поврзано железото, но не го содржи и самото железо.[1]
Уметникот Џулијан Вос-Андре создал скулптура наречена „Срце од железо (Хемоглобин)“ (англиски: Heart of Steel (Hemoglobin)) во 2005, заснована на градбата на белковината. Скулптурата била направена од стакло и железо. Намерното `рѓосување на првобитното сјајното уметничко дело ја прикажува основната хемиска реакција на кислородот кој се сврзува со железото.[2]
Рок бендот Placebo создаде песна наречена Хемоглобин (англиски: Haemoglobin) со стиховите „Хемоглобинот е клучен за здраво срцево чукање“.[3]
Наводи
уреди- ↑ Boh, Larry (2001). Pharmacy Practice Manual: A Guide to the Clinical Experience. Lippincott Williams & Wilkins. ISBN 0781725410.
- ↑ Holden, Constance (2005). „Blood and Steel“ (pdf). Science. 309: 2160. doi:10.1126/science.309.5744.2160d.
- ↑ Placebo - Haemoglobin (lyrics) (стиховите од песната)