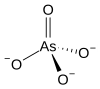
Арсенат
Арсенат — секое соединение кое го содржи арсенатниот јон AsO3−
4. Арсенатите се соли или естри на арсенската киселина.
Арсеновиот атом во арсенатот има валентност од 5 и се нарекува пентавалантен арсен или As(V).
Арсенатот во многу погледи наликува на фосфатот бидејќи арсенот и фосфорот се јавува во истата група (столб) на периоднот систем.
Арсенатите се умерени оксиданси, со електроден потенцијал од +0,56 V за редукција на арсенити.
| |||
Назив според МСЧПХ арсенат | |||
| Назнаки | |||
|---|---|---|---|
| 15584-04-0 | |||
| ChemSpider | 25498 | ||
| |||
| 3Д-модел (Jmol) | Слика | ||
| PubChem | 27401 | ||
| |||
| UNII | G1DBI405OK | ||
| Својства | |||
| Хемиска формула | |||
| Моларна маса | 0 g mol−1 | ||
| Конјуг. киселина | арсенска киселина | ||
| Дополнителни податоци | |||
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |||
| Наводи | |||
Застапеност
уредиВо природата, арсенатите се среќаваат во различни минерали. Овие минерали може да содржат хидрирани или безводни арсенати. За разлика од фосфатите, арсенатите не се губат од минералот при негово трошење. Примери за арсенатни минерали се адамитот, аларситот, анабергитот, еритритот и леграндитот.[1] Кога се потребни два арсенатни јона за рамнотежа на набојот во формула, тогаш спојот се нарекува диарсенат како кај трицинк диарсенатот (Zn3(AsO4)2).
Јони
уредиЗборот арсенат е добиен од арсенска киселина (H3AsO4). Оваа умерено силна киселина се пертвора во диводород арсенат (H2AsO−
4), водород арсенат (HAsO2−
4) и арсенат (AsO3−
4), зависно од pH-вредноста. Количествениот однос помеѓу овие видови е определен од константите на киселинската дисоцијација:
- H3AsO4 + H2O H2AsO−
4 + H3O+ (log K1 = −2.19) - H2AsO−
4 + H2O HAsO2−
4 + H3O+ (log K2 = −6.94) - HAsO2−
4 + H2O AsO3−
4 + H3O+ (log K3 = −11.5)
Овие вредности се слични на оние на водородните фосфати. Водород арсенатот и диводород арсенатот преовладуваат во воден раствор близу неутрална pH-вредност.
Труење со арсенат
уредиАрсенатот може да го замени неорганскиот фосфат во чекорот на гликолизата која произведува 1,3-бифосфоглицерат од глицералдехид 3-фосфат. Ова дава 1-арсено-3-фосфоглицерат, кој е нестабилен и бргу се хидролизира, образувајќи го следниот меѓупроизвод, 3-фосфоглицерат. Затоа, гликолиза се одвива, но АТФ-молекулата која би се создала од 1,3-бифосфоглицерат Се губи — арсенатот е одвојувач од гликолизата, што е причина за неговата токсичност.[2]
Како и останатите соединенија на арсенот, арсенитот се сврзува со липоинска киселина,[3] попречувајќи го претворањето на пируватот во ацетил-CoA, спречувајќи го Кребсовиот циклус, по што уследува понатамошна загуба на АТФ.[4]
Поврзано
уредиНаводи
уреди- ↑ Mineralienatlas - Mineralklasse Phosphate, Arsenate, Vanadate.
- ↑ Hughes, Michael F. (2002). „Arsenic toxicity and potential mechanisms of action“. Toxicology Letters. 133 (1): 1–16. doi:10.1016/S0378-4274(02)00084-X. PMID 12076506.
- ↑ Stone, Taylor J. (декември 2008). „Biochemistry of Arsenic Poisoning“. Архивирано од изворникот на 20 март 2018. Посетено на 21 август 2022.
- ↑ Kim Gehle; Selene Chou; William S. Beckett (1 октомври 2009), Arsenic Toxicity Case Study, Agency for Toxic Substances and Disease Registry