Комплекс (хемија)
Комплексни или координациони соединенија се такви соединенија во чиј состав влегуваат комплексни честички изградени од повеќе атоми, молекули или јони, кои градат една стабилна групација во цврста агрегатна состојба и/или во раствор.
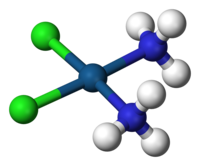
Атом на платина со четири лиганди
Комплексните честички се изградени од централен атом (или комплексообразувач) и лиганди. Централниот атом е некој метал или метален катјон кој нема пополнета електронска конфигурација на инертен гас. Лигандите се најчесто анјони или неутрални молекули што содржат еден или повеќе неподелени, односно слободни електронски парови. Многу ретко како лиганди можат да се јават и катјони, но такви што содржат неподелен електронски пар на некој од атомите. Како и да е, централните атоми се Луисови киселини, а лигандите се Луисови бази.
Кога се пишуваат хемиските формули на комплексите, прво се пишува симболот на централниот атом, а потоа анјонските и неутралните лиганди. Формулата на комплексот се пишува во аглести загради. Во името прво се наведуваат анјонските лиганди, потоа неутралните и катјонските лиганди, а на крај името на централниот атом. Бројот на лигандите се искажува со грчките претставки ди, три, тетра, пента итн. (а бројот на лигандите се означува со пртставките бис, трис, тетракис итн.), а името на лигандата се пишува во мали загради. Оксидационата состојба на централниот атом се искажува со Стоксова нотација (римски бројки во мали загради). Имињата на катјоните и анјоните кај комплексите се пишуваат слеано, со сите претставки, имињата на лиганди и централниот атом.
Постојат разлики во именувањата на централниот атом кај комплексните катјони и анјони. Така, кај комплексните анјони, од латинското име на централниот атом се отфрла наставката ум или иум, а се додава наставката ат (исклучок се комплексите на живата, каде се употребува англиското име - меркурат). Кај катјонските и неутралните комплекси, централниот атом се именува на македонски без никаква наставка.
Имиња на лигандите уреди
Имињата на анјонските лиганди завршуваат на о. Општо, ако името на анјонот завршува на ид, ит или ат, се додава о и така се добива идо, ито или ато, соодветно. Исклучок од ова правило прават некои соединенија, кај кои се отфрла ид, а се додава о.
Имињата на лигандите што се молекули се употребуваат без промени. Водата и амонијакот се именуваат како аква и амин, соодветно.